�����ο�Ȯ�����ɂο�Ȯ����������İ�����N�����Ұ������l����һ�N���Ԃ�Ⱦ�����ο�Ȯ���������ڰ�����ƣ����Ͱ�������ơ���Ⱦ�ԵIJ������Ă���ͬ�ĽY���M�ɣ��քe��(�D1)�������о�ɾ����p� DNA �M�ɣ�DNA ͬ�������ϵľ��б��o�ԵĶ�ʮ���w�Π������ͬ���ɺ������ɵ����|�����g�|Ƕ�����У�����ӱ��ɶ�N�����ǵ��M�ɵ���Ĥ������
�����D1 �ο�Ȯ�����Y��
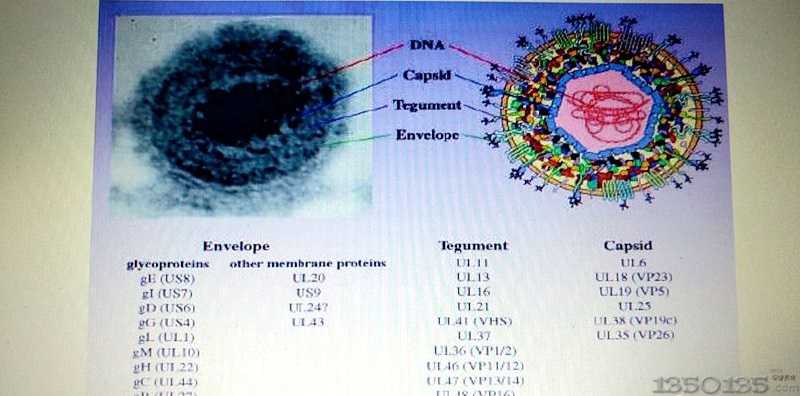
����1���˽�ο�Ȯ��������M�Y�����������P���Ĺ���
�����ο�Ȯ��������M���p��DNA����С��150kb�����L���^(UL)�Ͷ̪��^(US)�Լ�US�ɂȵ�ĩ���؏�����(TR)�c�Ȳ��؏�����(IR)���M�ɡ�Ŀǰ�ѽ�֪�����첡��������50�N�����|������������11�N�ǵ��ף������c�������P���ǵ�����gC��gD��gE��gl�����⣬���ռ�ø(TK)��������߀ԭø(RR)������ø(��PK)���A�Ժ�������ø(AN)��Ó����������3�ἤø(dUTPase)�ȎNøҲ�c�����Ķ����������P�������ǛQ�������Ƿ�����������l�����������P�I�����أ��ο�Ȯ�Ķ����ɶ�������Q�����˽��@Щ�����������҂����Ƴ����͂ο�Ȯ���磬�����ο�Ȯ����Σ�����@Щ������Ҫ��������(��1)��
������1 �c�ο�Ȯ�������������P�ĵ���

����2��TK�����ȱʧ�����Л]�ЬF�����x?
�������1��ʾ��TK�������c�������P����Ҫ����֮һ�����c�����ď��ơ�������Ⱦ���P�����о�����TK�����ȱʧ��ʹ�䌦�i�ͷ��c����Ķ����@�����ͣ�ͬ�r������Ⱦ����Ҳ�½������TK�����ȱʧ��ɞ��˂��о��Ľ��c��Kit��1948������BUK��_��TK����Ȳ�148bp�Ƴ����磬ԓ����]�г��F�����؏ͬF���i�ṩ����Ч���o���ڇ��ȣ��Ĵ��r�I��W������Fa��TK����ȱʧ�磬�ӷNС�iҲ�@ʾ�˺ܺõ�����Ч�����b���@Щ���ڵ��о��ɹ����ܶ�����S�Ҷ���TK����ȱʧ����A�аl�������磬��ǰTK�����ȱʧ����ЬF�����x��?
�����mȻTK�����ȱʧ�����˲����Ķ���������Ժ��������S����TK����ȱʧ�аl����������Ҳ�@ʾ��һ��Ч������TK�����ȱʧ����һ�����������ؽM���L�U��������ԭ��Ҳ���ܵ�Ӱ푡�������о�������ijЩ�����������ֲ�������i���[�нM����������Ԫ����ͨ�^�c�ο�ȮҰ���ij���Ⱦ�������Ķ�����[�Ը�Ⱦ�İl�����о�߀������ȱʧTK�����������������������ֲ�������]�С������͜p��Ұ�������Ը�Ⱦ�ڂο�Ȯ���ķ����������P��Ҫ�ġ�
�����о��������Ϊ�ͨ�^�����ֶ�ȱʧTK�����䲡���Ķ���߀�Ǵ���һ���֣����i����һ�����L�U����Ŀǰ�����ϰ�ȫ��Ч���������綼��ͨ�^���͂������B�@�ã�ͨ�^���ɴ������B���Ķ�������l��һЩͻ׃������Ƚ����˲����Ķ��������`�C���@�ӵ���Ȼ������ʽ���ǰ�ȫ��Ч�ġ��H�Hͨ�^�����ֶ��õ�TK�������R��������߀�Ǖ�����һ���L�U��
����Ŀǰ�аl�ο�Ȯ����ȱʧ����ҪĿ�����b�e�����i��Ұ����Ⱦ�i��������i���ο�Ȯ���ṩһ�N�O�y�ֶΡ��mȻ�ӷNTK����ȱʧ�磬�i�ܮa�����ĵֿ��ο�Ȯ�����Ĺ�����������TK�������ø���������w�Ȳ��ܮa�������Ŀ��w����˲�����Ѫ��W�����^�e���߽ӷN�i�c��Ȼ��Ⱦ�i��
����ͨ�^����Փ�C�����Կ�����TK����ȱʧ�������аl�ο�Ȯ����ȱʧ����A�]�ЬF�����x��
����3��gE�����ȱʧ�������ЬF�����x��
������D1��ʾ��gE����Ҳ�ǂο�Ȯ����һ����Ҫ�Ķ��������ڂο�Ȯ��������ϵ�y�ĔUɢ������Ҫ���á��о��l�F��ֻҪȱʧ��gE 5’�˵�125λ���i����͵�126λ�İ��װ��ᣬ�ο�Ȯ���������͕�����Ҳ�Ӱ�������ԭ�ԡ�gE�ǵ���N��33λ��100λ�İ�����^�ΰ�������Ҫ��ԭ��λ��ȱʧ��ԓ�λ����ڙC�w�ȾͲ��ܮa�������ĺ��w���@��^�eҰ����Ⱦ������ӷN�ṩ��������
����������gE����ȱʧ�ѽ��ɞ�������о����c��Quint�Ȍ��ο�ȮNIA-3���M��gE����ȱʧ�������Ăο�Ȯͻ׃�������@���͌�С���10���g���i�Ķ����������i�ֿܵ��������������������ȣ��Ĵ��r�I��WҲ�ɹ�������gE/gI����ȱʧ�꣬�@ʾ�����õ�����Ч����������Ĵ��̈́���������˾ҲͶ������������������аl��gE����ȱʧ����A���������硣
�������i���ij�Ҏ�����^���У���ͨ�����ڽӷN���mȻ���A���R���Y��ij��F�������ܷ�ֹ�����ڱ���Ⱦ�����w�ȏ��ơ��ų����˕r����gE����ȱʧ�������߲��Y��gE-ELISA�z�y��gE���w��^���_�ӷNѪ������i��Ұ����ȾѪ������i���@�N�ӷNgE����ȱʧ����Y���b�e���\�������F���ѳɞ�������������^�ƏV�Ăο�Ȯ������Ӌ������Փ���A�������f�аl�Ԃο�ȮgE����ȱʧ����A����������ЬF�����x��
����4���Y
�����C�������������͜p��Ұ�������Ը�Ⱦ�������p����Ұ���b�e�������濴��TK����ȱʧ�������аl�ο�Ȯ����ȱʧ����A�]�ЬF�����x���ο�Ȯ���ă���֮·���ض����h�������b�eҰ�������Ăο�Ȯ����ȱʧ��ij��F�҂�������ϣ����Ȼ��TK����ȱʧ�猦�ڂο�Ȯ�ă������κ����ã������͜p��Ұ�������Ը�Ⱦ������]�����ã��R������Ҳ����һ���L�U���cgE����ȱʧ���TK�C�������������͜p��Ұ�������Ը�Ⱦ�������p����Ұ���b�e�������濴��TK����ȱʧ�������аl�ο�Ȯ����ȱʧ����A�]�ЬF�����x���ο�Ȯ���ă���֮·���ض����h�������b�eҰ�������Ăο�Ȯ����ȱʧ��ij��F�҂�������ϣ����Ȼ��TK����ȱʧ�猦�ڂο�Ȯ�ă������κ����ã������͜p��Ұ�������Ը�Ⱦ������]�����ã��R������Ҳ����һ���L�U���cgE����ȱʧ���TK����ȱʧ�]�ЬF�����x��
����Ŀǰ�i�����߂ο�Ȯ�����^��ʹ�û���ȱʧ�磬���ǻ���ȱʧ��Ҳ���^��ķ���Іλ���ȱʧ�ģ�Ҳ�ж����ȱʧ�ģ��i������ԓʹ���ķN���磬�@��Ŀǰ��Փ�^��Ć��}�������J�R�@�����}�����X�ÿɏ��������������
����1�������ȱʧ�粻���ڶ��r��
�����@����ͨ���R�����r���Ǻ��ж�N��ԭ�ɷݣ����ߺ��i�ṩ����ı��o�������ȱʧ��t��ȱʧ�������p����һЩ��ԭ�ɷݡ���Ȼ�p�ٵ��@Щ��ԭ�ɷ����w������Ч��Ӱ푲���
����2������ȱʧ��Ŀ��
��������ȱʧ����ҪĿ���Ǟ����b�e�����i��Ұ����Ⱦ�i��������ο�Ȯ���ṩѪ��W�O�y������Ŀǰ������ͨ�õ���gE�ο�¡���wELISAԇ���У��λ���ȱʧ��Ͷ����ȱʧ�綼��ͨ�^��ԇ�����_���b�eĿ�ģ����@һ���x�ρ��f�����ߛ]���κ΅^�e��
����3��������
������Ŀǰ��ֹ��߀�]�Й����Ե�Փ�����λ���ȱʧ��Ͷ����ȱʧ������Ч��֮�g�ă������^�u���������˽�ĸ��i�����H���ÿ������ߌ����Ƃο�Ȯ�����������õ�Ч�������wˮƽ�ıO�yҲ�]�аl�F����֮�g���ڲ��������о�������ijЩ�����������ֲ�������i���[�нM����������Ԫ����ͨ�^�c�ο�ȮҰ���ij���Ⱦ�������Ķ�����[�Ը�Ⱦ�İl�����о�߀��������ȱʧ�ǵ���gE��ȱʧTk�����������������������ֲ�������������͜p��Ұ�������Ը�Ⱦ�ڂο�Ȯ���ķ����������P��Ҫ�ġ�
����4����ȫ��
�����@���p����Փ�Ľ��c���}����Ҫ���P�چλ���ȱʧ���Ƿ�ȫ�Ġ�Փ��
��������ȱʧ�ڜp��������һ�����ã����@Ȼ�dz����ޣ������ߌW�Ƕȁ���������Ĝp����Ҫ߀����ه���^�����B��Ŀǰ���ο�Ȯ�������⣬�������綼�]��ȱʧ�������м�����������ʮ��N���i���������塢���N�������������ߡ��˷N������f�@Щ������ڶ���������������ȫ�Ԇ��}���@Ȼ�c����������ˣ��������ijһ�N����ȱʧ�����^�ֿ�����ȱʧ�ڰ�ȫ�Է�������ã������ѻ���ȱʧ�Ķ����������һ�����簲ȫ�Ե�������
�����Ěvʷ�ĽǶȿ����λ���ȱʧ����(��Bartha��)��һ��ʹ�Úvʷ���L(1961�����Ƴɹ�)��������V�����������������硣��������ʮ����đ��Ì��`�ѽ������@��һ���������Ͱ�ȫ�Զ��ܺõ������ꡣ��ˣ������������ȱʧ��(��ͬ�rȱʧTK����)���{�䰲ȫ�Ծͷ��^����Ɇλ���ȱʧ��İ�ȫ�ԣ��@�c˼�S߉���������c�l������������
�����ĬF���ĽǶȿ����λ���ȱʧ����Ȼ�����緶�����Á����Ƃο�Ȯ������ҪƷ�N����ʮ��ע�����ﰲȫ�ĚW�����ң����a��ʹ��һ�N����ȫ�������������y������ġ�
������Ŀǰ��ֹ�����Ў������˾��Bartha��λ���ȱʧ������@�����҇��r�I��������ע�ԣ��������S�M�ڡ��҇�Ҳ��һ��Խ��Խע�����ﰲȫ�ć��ң�����ע���@Щ�λ���ȱʧ��r���Ǐĸ��������ֿ��]���J�C���䰲ȫ�����أ��@Ȼ���P�λ���ȱʧ����������ڰ�ȫ���}���f������ȫ�����ŵġ�
�����Ϸ�ijijʡ��ʮ��Ҏģ���i����1999����_ʼʹ�Æλ���ȱʧ�����磬����δ�l����ȫ�Ԇ��}�����ɷ��J�����Ђ��e�i����ʹ�Æλ���ȱʧ��������FһЩ���}����������ҙz�y�����}�������磬����ԓ�i���ڽӷN����r�ѽ���Ⱦ��������ֳ�ϵK�Լ������i���ˆTҲ��ʾ���ӷN������ѽ��І��}�l�����@�NżȻ��r��������͵�����ʹ���^����Ҳ��������